- Betriebsmanagement
- Messinstrument
- Wasser-Analysator
- Stelzner/ Pronova Analysentechnik GmbH&Co.KG
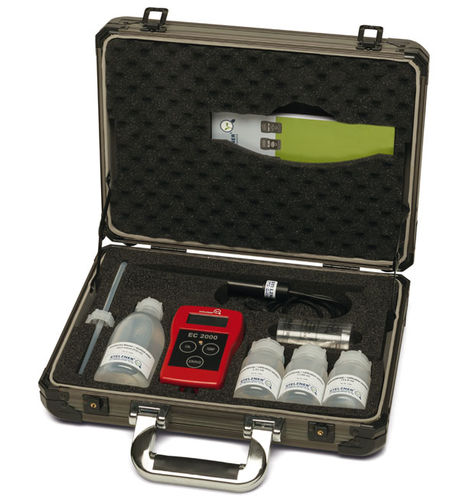
Wasser-Analysator EC 2000für Nährlösungelektrisch leitendtragbar
Zu meinen Favoriten hinzufügen
Zum Produktvergleich hinzufügen
Eigenschaften
- Analysiertes Produkt
- Wasser, für Nährlösung
- Messwert
- elektrisch leitend
- Bewegbarkeit
- tragbar
Beschreibung
Leitfähigkeitsmessung in Lösungen
Die elektrische Leitfähigkeit bestimmt den elektrischen Strom zwischen zwei Punkten (Elektroden) mit unterschiedlichem Potenzial (Spannung), z.B. in einer Flüssigkeit. Je mehr Salz, Säure oder auch Base eine Messlösung enthält, desto höher ist deren Leitfähigkeit. Die Einheit für die Leitfähigkeit ist mS/cm. Die Skala für wässrige Lösungen beginnt bei reinstem Wasser mit einer Leitfähigkeit von 0,05 µS/cm (25 °C) und endet bei einigen Basen bei 1,0 mS/cm (z.B. Kaliumlösungen). Natürliches Wasser, wie Trinkwasser oder Oberflächenwasser, liegt im Bereich von 0,1 bis 1,0 mS/cm.
Die Messung der Leitfähigkeit erfolgt über eine Messzelle, die im einfachsten Fall aus zwei gleichartigen Elektroden besteht. Eine an die Elektrode gelegte Wechselspannung führt zu einer auf die Elektrode ausgerichteten Bewegung der in der Messlösung enthaltenen Ionen. Je mehr Ionen die Messlösung enthält, desto größer ist der zwischen den Elektroden fließende Strom. Das Messgerät berechnet aus dem gemessenen Strom zunächst den Leitwert der Messlösung und danach unter Einbeziehung der Zelldaten den Leitfähigkeitswert.
Kataloge
Weitere Produkte von Stelzner/ Pronova Analysentechnik GmbH&Co.KG
Leitfaehigkeit
Verwandte Suchbegriffe
- Elektronische Waage
- Tragbarer Analysator
- Wetterstation
- Feuchteanalysator
- Digitaler Analysator
- Temperatur-Wetterstation
- Kabellose Wetterstation
- Bodensonde
- PH-Analysator
- Feuchtesensor für Böden
- Benchtop-Analysator
- Temperatur-Datenlogger
- Automatische Waage
- Tragbare Bodensonde
- Windrichtungs-Wetterstation
- PH-Meter
- Refraktometer
- °C-Thermometer
- Analysator für Boden
- Digitaler Feuchtesensor
* Die Preise verstehen sich ohne MwSt., Versandkosten und Zollgebühren. Eventuelle Zusatzkosten für Installation oder Inbetriebnahme sind nicht enthalten. Es handelt sich um unverbindliche Preisangaben, die je nach Land, Kurs der Rohstoffe und Wechselkurs schwanken können.





